解读癌症和HIV新型实验性/候选药物研究进展
本文中,小编整理了相关的研究进展,共同解读近年来癌症和HIV研究领域新型候选/实验性药物的最新进展情况,分享给各位!
【1】潜在的候选药物可阻止前列腺癌和乳腺癌生长
斯克里普斯研究所(TSRI)佛罗里达校区的科学家们设计了两种新的候选药物靶向前列腺和三阴性乳腺癌。
最近在ACS中央科学和美国化学学会杂志上发表的两项独立研究的新研究表明,一类称为小分子RNA抑制剂的新型药物可以成功靶向和杀死特定类型的癌症。
一种抗前列腺癌的工具
RNA是将我们的遗传密码翻译成蛋白质的分子。RNA缺陷可导致癌症,肌萎缩性侧索硬化(ALS),强直性营养不良和许多其他疾病。
在他们的ACS中央科学研究中,迪斯尼和他的同事使用DNA测序来评估成千上万的小分子。研究人员正在寻找可以与缺陷RNAs类似的钥匙精确结合的分子。
【2】Cancer Cell: 科学家揭示肺腺癌治疗新靶点 候选药物已进入临床试验阶段
DOI:10.1016/j.ccell.2016.12.010
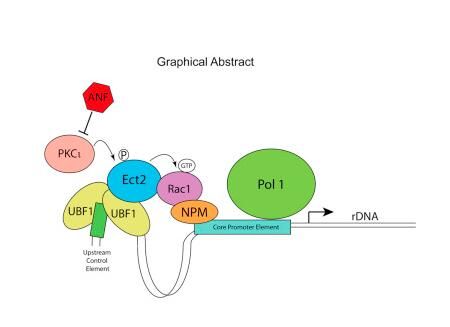
美国梅奥诊所的研究人员发现一个癌基因能够促进肺癌发生。相关研究结果发表在国际学术期刊Cancer Cell上,梅奥诊所的研究人员提供证据表明Ect2能够驱动肺腺癌肿瘤形成。
“这篇文章首次确定了Ect2能够参与体内肿瘤形成,还发现了Ect2在肺腺癌细胞中的一个与核糖体有关的新功能。”文章高级作者Alan Fields这样说道。Dr. Fields是一位癌症生物学家,也是梅奥诊所癌症生物学部的一位教授。
肺癌中的KRAS突变
据Dr. Fields介绍肺癌病人中有大约40%被诊断为肺腺癌。驱动这种癌症发生的最常见因素就是KRAS基因突变。“KRAS介导的肺腺癌是一种特别致命的肺癌类型,其中部分原因在于直接靶向KRAS的治疗方法并未在临床上取得成功。”该研究作者Verline Justilien教授这样表示。

【3】Cell子刊:科学家开发出新的抗体药物偶联药治疗癌症
doi:10.1016/j.chembiol.2017.02.012
来自斯克里普斯研究所(TSRI)佛罗里达校区的研究人员近日开发出了一种新型药物递送系统,在治疗动物肿瘤模型(包括难治的实体瘤和血癌)时取得了良好的结果。这项研究由TSRI副教授Christoph Rader领导完成,相关成果近日发表在Cell Chemical Biology上。
这种新方法涉及一种叫做抗体-药物键合物(ADCs)的药物,ADCs包含一些最具有潜力的下一代抗体抗癌药物。ADCs可以高度选择性输送毒性药物到肿瘤组织。迄今为止,已经有3种ADCs被FDA批准,但是这些ADCs将药物键合在抗体的位置并没有确定。
“我们已经在这项技术上花了不少时间了。”Rader说道,“这种方法是基于很少用的天然氨基酸——硒代半胱氨酸,我们将这种氨基酸插入到抗体中,我们将这些工程化抗体称为selenomabs。”
抗体是大的免疫系统蛋白,可以识别肿瘤细胞上的特定分子标记物——抗原。抗体本身清除肿瘤的能力并不强,但是它们对抗原的高度特异性使它们成为了直接输送药物到肿瘤的理想载体。
【4】新型测试药物或有望激活机体免疫系统 高效抵御癌症
新闻阅读:Investigation tests drug to activate immune system, help fight cancer
科学家们利用抗体药物复合体治疗癌症已经有一段时间了,但这也暴露出了一些问题,目前研究人员无法模拟出机体内部癌细胞的形状,有时候甚至会产生不正确的研究结论,来自国际空间站的特殊微重力环境或许就能够帮助科学家们从新型的3D角度来进行研究。
研究者在微重力的环境中调查Azonafide抗体药物复合体(ADCs)的功效和代谢状况,目的就是去刺激癌细胞内免疫性细胞的死亡,这或许就能够消灭癌症并且抑制未来疾病复发,当然相关研究或许也为会研究人员提供一种新型的药物和抗体组合,从而增加疗法的效率,并且降低化疗相关副作用。
研究者Luis Zea说道,在宇宙空间中,我们可以生长出越来越大的球形肿瘤结构,因此我们就有了一种很好的模型来研究其在人类机体中的作用,当然产生假阴性或假阳性结果的机会就会相应降低。阐明药物组合如何在微重力环境中发挥作用对于研究人员后期开发出治疗诸如癌症等疾病的新型疗法非常关键。

【5】JCMM:男性避孕候选药物居然可治愈睾丸癌!
DOI:10.1111/jcmm.13059
睾丸癌是20-40岁之间男性最常见的恶性肿瘤,通常可以治愈。但是很不幸,现有药物仍然对一些病人的肿瘤无治疗效果。而最新研究发现一种本来用于避孕的药物居然为这些患者带来了新希望,此前研究人员发现这种叫做JQ1的试验性药物可以抑制精子成熟,因此可能是一种男性避孕候选药物。但是现在研究人员发现它还可能用于治疗睾丸癌。
JQ1属于一类作用强大的药物:该类药物成员可以从根本上影响基因的表达活性。遗传物质DNA是一种复杂的分子,其中包含指导合成蛋白质的序列,这些DNA与组蛋白组装成串珠状结构保存在细胞核中。
但是组蛋白不仅只发挥结构上的作用,它们还有调控基因表达的功能。组蛋白上充满了化学标签——甲基或者乙酰基,这些标签决定了DNA转录系统是否可以识别对应部位的DNA并进行转录。“JQ1可以抑制转录蛋白识别这些标签,从而改变这些基因的表达活性。”来自波恩大学病理学研究所的Hubert Schorle教授解释道。
【6】Nature:重大发现!实验性药物GGTI-2418抑制肿瘤生长
doi:10.1038/nature22965
美国莫非特癌症研究中心药物研发部主任Said M. Sebti博士及其团队和美国纽约大学朗格尼医学中心生物化学与分子药理学系主任Michele Pagano博士及其团队领导的一项新的研究发现药物香叶基香叶基转移酶(geranylgeranyltransferase)抑制剂GGTI-2418抑制Pagano团队发现的一种新的存在缺陷的PTEN癌症通路。相关研究结果于2017年6月14日在线发表在Nature期刊上,论文标题为“PTEN counteracts FBXL2 to promote IP3R3- and Ca2+-mediated apoptosis limiting tumour growth”。
众所周知,完全功能性的PTEN通过抵抗PI3K/Akt肿瘤存活通路来抑制肿瘤生长。Pagano团队发现一种新的机制:PTEN通过阻止香叶基香叶基化的蛋白FBXL2结合和降解IP3R3来阻止细胞发生癌变。IP3R3是一种重要的抗癌“检测器”,能够识别过度增殖的细胞(这些细胞消耗异常高水平的能量),并且作为一种抗癌安全机制靶向它们以便让它们自我摧毁。PTEN结合到IP3R3上,保护它的癌症检测功能。然而,PTEN在很多癌症中是存在缺陷的,也因此FBXL2不受其监管;太多的IP3R3遭受降解,而且快速增值的细胞更不能够发生自我摧毁。
【7】Mol Can Therap:实验性抗癌药物TAK-733或是新一代杀灭黑色素瘤的利器
doi:10.1158/1535-7163.MCT-13-1012
近日,刊登在国际杂志Molecular Cancer Therapeutics上的一项研究成果中,来自科罗拉多大学癌症研究中心的研究人员通过利用一种名为TAK-733的实验性药物对植入人类肿瘤样本的小鼠进行试验,发现该药物对11只小鼠中的10只都具有抗癌活性。
TAK-733是MEK1/2分子的抑制剂,TAK-733被设计为治疗携带BRAF突变病人疾病的第二代治疗抑制剂,而本文研究揭示了TAK-733对黑色素瘤模型也具有效应而不论个体机体是否携带BRAF突变。
John Tentler博士表示,这种新型药物分子的重要性在于其是新一代高效抑制黑色素瘤的潜在抑制剂,其可以有效杀灭黑色素瘤,而本文研究中利用TAK-733对植入肿瘤组织样本的小鼠的研究结果也使得我们对人类机体中的试验结果很有希望。
【8】Mol Ther:一种实验性药物可越过肿瘤血脑屏障 靶向杀灭肿瘤细胞
doi:10.1038/mt.2013.114
近日,刊登在国际杂志Molecular Therapy上的一篇研究报告中,来自俄和俄州立大学癌症研究中心的科学家通过研究发现,在早期恶性脑瘤研究中的一种实验性药物,可以绕过血脑肿瘤屏障,杀灭肿瘤细胞并且阻断肿瘤血管组织的生长。
在文中研究者揭示了这种名为SapC-DOPS的制剂如何对肿瘤细胞及血管进行靶向作用,相关研究或为开发新型治疗脑瘤的药物提供思路和希望。多形性胶质母细胞瘤是一种常见的恶心脑瘤,患者的生存中值大约为15个月。
研究者Balveen Kaur教授表示,很少有药物可以越过肿瘤组织的血脑屏障来对肿瘤细胞进行靶向杀灭作用,我们的前期临床试验揭示,SapC-DOPS的确可以抑制新的肿瘤血管组织的形成,这也就表明SapC-DOPS终有一天可以用于治疗多形性胶质母细胞瘤及其它实体瘤。
【9】Nat Med:重磅级研究!新型抗体药物或有望彻底治疗HIV感染
doi:10.1038/nm.4268
近日,来自洛克菲勒大学的研究人员开发出了一种新型的生物制剂,其或许有望作为靶向作用HIV的潜在疗法,相关研究刊登于国际杂志Nature Medicine上;这种名为10-1074的药物或许就能够为研究人员提供一种新方法来抑制HIV高风险个体机体的病毒感染。
研究者表示,这种药物属于广谱中和性抗体(broadly neutralizing antibodies, bNAbs),这类抗体天然状况下存在于HIV感染者机体中,虽然有这种抗体,但患者机体的免疫系统却并不能有效抵御病毒;研究人员Till Schoofs说道,这项研究是药物10-1074进行的首个人类临床试验,相比其它抗体而言,该抗体能够同病毒的不同部位结合,此外,该抗体也是目前研究人员鉴别出的最具有潜力的广谱中和性抗体。
如今研究人员能够利用抗逆转录病毒疗法来抵御HIV感染,这种抗逆转录病毒疗法体系在20世纪90年代开始使用,尽管其能够挽救很多HIV感染者的生命,但抗逆转录病毒药物也存在一些明显的缺点,其往往会引发一些副作用,而且患者需要终生服药,这就是为何研究人员需要继续寻找方法来抵御HIV的原因了,研究人员希望能够利用广谱中和性抗体来作为一种治疗HIV感染的替代性疗法。
【10】JCI:URMC-099可延长HIV药物的疗效
doi:10.1172/JCI90025
美国罗切斯特大学医学中心开发的一种药物启动细胞自身抵抗HIV的防御机制,从而延长多种HIV药物的疗效。在开发能够每年服用一到两次就可长期发挥疗效的药物的目标上,这一发现迈出了重要的一步,而在当前,病人必须每天服用HIV药物。相关研究结果于2017年1月30日发表在Journal of Clinical Investigation期刊上,论文标题为“Autophagy facilitates macrophage depots of sustained-release nanoformulated antiretroviral drugs”。
这种被称作URMC-099的药物是由罗切斯特大学医学中心科学家Harris A. Gelbard博士实验室开发的。当与两种常用的抗HIV药物(也被称作抗逆转录病毒药物)纳米制剂版本组合使用时,URMC-099启动一种被称作自噬的过程。
正常情形下,自噬允许细胞清除胞内的“垃圾”,如入侵的病毒。当HIV感染时,这种病毒阻止细胞启动自噬,这也是它为了存活所采用的众多诡计之一。当启动自噬时,细胞能够消化在接受抗逆转录病毒药物治疗后残存下来的任何病毒,从而让细胞在更长的时间内免受病毒感染。(生物谷Bioon.com)
版权声明:本文系生物谷原创编译整理,未经本网站授权不得转载和使用。如需获取授权,请点击 
生物谷更多精彩盘点!敬请期待!