前瞻生物医药产业全球周报2022第11期:第一三共出售在华业务,赛诺菲和IGM


 第一三共出售在华业务
第一三共出售在华业务
4月1日,第一三共(中国)与重庆药友制药有限责任公司签署股权转让协议,并在其官方微信公众平台发布了相关转让信息。根据发布的信息显示,第一三共(中国)向重庆药友转让大陆地区可乐必妥制剂的生产销售权和生产该制剂的生产公司全部股权,预计将于今年8月底完成转让。对于本次交易转让价格,第一三共(中国)并未公开。
赛诺菲和IGM Biosciences达成逾60亿美元合作
近日,赛诺菲和IGM Biosciences公司宣布达成研发合作,将利用IGM Biosciences公司独有的IgM抗体技术平台,开发针对三个肿瘤学靶点和三个免疫学/炎症靶点的激动剂。
 CDE发布《胰岛素类产品生物类似药药学研究与评价技术指导原则》
CDE发布《胰岛素类产品生物类似药药学研究与评价技术指导原则》
近日,CDE官网发布了一则《胰岛素类产品生物类似药药学研究与评价技术指导原则》的通告(2022年第22号)。该指导原则适用于采用重组技术表达、制备的七种胰岛素类产品的生物类似药,包括:人胰岛素、甘精胰岛素、门冬胰岛素、赖脯胰岛素、谷赖胰岛素、地特胰岛素和德谷胰岛素。其复方制剂以及经其他改构设计或化学修饰的胰岛素类产品可酌情参考本指导原则。
 腾盛博药与国药控股达成合作 共同商业化新冠中和抗体
腾盛博药与国药控股达成合作 共同商业化新冠中和抗体
30日,腾盛博药宣布,其子公司腾盛华创与国药控股达成战略合作,双方将共同携手推进公司长效新冠单克隆中和抗体安巴韦单抗/罗米司韦单抗联合疗法在中国的商业化进程,包括药品储备、渠道分销、区域准入、及其它创新业务合作。
对奥密克戎变异株无效 FDA修订GSK/VIR新冠抗体疗法EUA说明书
葛兰素史克与合作伙伴VIR Biotechnology近日联合宣布,美国FDA已修订了单抗药物sotrovimab的紧急使用授权(EUA)情况说明书。FDA已经确定,基于所有可用证据,包括VIR产生的新的活病毒数据,sotrovimab 500mg剂量不太可能对奥密克戎BA.2(Omicron BA.2)变异株有效。
3家企业主动申请降低新冠检测试剂部分产品中选/挂网价格
29日,广东省药品交易中心发布通知,日前,有3家《新型冠状病毒(2019-nCoV)检测试剂联盟地区集团带量采购》中选企业主动申请降低其部分产品中选/挂网价格。具体包括:新冠病毒(2019-nCoV)核酸检测试剂盒(荧光PCR法)由每人份9.1元调整为8元;新冠病毒(2019-nCoV)抗原检测试剂盒(胶体金法)价格,由每人份9.8元调整为7.9元;新冠病毒(2019-nCoV)核酸检测试剂盒(荧光PCR法)中选价格,由每人份9.81元调整为8元。
广东再次开展省际联盟集采!针对新型冠状病毒检测试剂耗材
近日,广东省药品交易中心发布了《关于开展广东联盟新型冠状病毒(2019-nCoV)检测试剂耗材相关品种预报名工作的通知》,通知显示,将开展广东联盟新型冠状病毒(2019-nCoV)检测试剂耗材相关品种预报名工作。品种范围包括:获得有效国内医疗器械注册(备案)证的新型冠状病毒(2019-nCoV)核酸、IgM抗体、IgG抗体、IgM/IgG抗体、总抗体、抗原检测试剂盒,以及新型冠状病毒检测配套的核酸提取或纯化试剂类、样本采集器具类、疫苗接种注射器类医用耗材。
第三批津冀新冠抗原检测试剂挂网采购价格公布
30日,天津市医药采购中心公布第三批津冀新冠抗原检测试剂挂网采购价格。其中,乐普诊断新型冠状病毒(2019-nCoV)抗原检测试剂盒(胶体金法)为9元/人份,万孚生物为7.9元/人份。
Novavax向欧盟申请扩大新冠疫苗授权范围 用于12-17岁青少年
日前,Novavax宣布在欧盟提交了针对12-17岁青少年注射COVID-19疫苗Nuvaxovid(NVX-CoV2373)的有条件上市许可申请。如果最终能够获得批准,该疫苗将成为欧洲市场针对12-17岁青少年的第一款蛋白质新冠疫苗。
新冠病毒疫苗费用1200余亿元由医保基金和财政共同分担
2日,国家医保局表示,目前,我国已经接种32亿剂次疫苗,疫苗费用1200余亿元,由医保基金和财政共同分担,疫苗支出费用在医保基金可承受范围内。
 企业合作
企业合作
首付款总计4500万美元 信达生物获礼来两款产品中国商业化权益
28日,礼来公司和信达生物宣布将深化战略合作,就以下事项达成协议:1)授予信达生物在中国大陆进口、销售、推广和分销VEGFR-2单抗希冉择(雷莫西尤单抗)和RET抑制剂Retsevmo(塞普替尼)获批后独家商业化权利;2)授予信达生物享有BTK抑制剂pirtobrutinib未来在中国大陆商业化权利的优先谈判权。根据协议,待雷莫西尤单抗肝细胞癌适应症以及塞普替尼非小细胞肺癌适应症获批注册后,信达生物将支付礼来公司总计4500万美元的首付款。信达生物将在雷莫西尤单抗和塞普替尼获批后负责在中国销售。
华润生物医药与优锐生物达成合作
28日,华润医药子公司华润生物医药宣布与优锐生物就精准靶向和整体免疫激活项目PTIA1在全球范围内的产品合作开发达成独家合作,并签署了合作协议。
超2.3亿美元!博奥信生物抗Siglec-15抗体实现海外授权
30日,博奥信生物宣布与Pyxis Oncology签订授权协议。根据协议,Pyxis Oncology将获得博奥信生物创新抗体BSI-060T除大中华区外的全球开发和商业化独家许可,博奥信生物将获得1000万美元的首付款,还将有资格收到总额高达2.225亿美元的里程碑付款,以及销售额中高达两位数比例的特许权使用费。
人事变动
辉瑞消化系统/泌尿/血液肿瘤负责人确定 来自
近日,有消息爆料称,褚楠女士被任命为辉瑞消化系统/泌尿/血液肿瘤治疗领域负责人,工作地点在上海,该任命于2022年3月28日起正式生效。在加入辉瑞之前,她在上海君实生物担任市场营销与医学事务副总裁,负责肿瘤产品组合战略,创新药出海国际化战略。
先声药业任命Danny Chen为集团高级副总裁
28日,先声药业宣布,任命Danny Chen为集团高级副总裁,负责推进公司转化科学与神经领域研发工作,以及北京创新中心研发团队组建与管理,增强先声在中枢神经治疗领域的全球研发能力。
三位副总经理离任
30日,华兰生物发布公告称,公司高管发生人事变动。具体事项如下:①潘若文离任副总经理职位,离任时间为2022年3月29日,离任原因为:因工作变动原因。②王启平离任副总经理职位,离任时间为2022年3月29日,离任原因为:因退休原因。③安文琪离任副总经理职位,离任时间为2022年3月29日,离任原因为:因工作变动原因。据了解,安文琪于2018年3月26日起在公司担任该职位。
Jeff Porter出任来凯医药科学顾问委员会主席
29日,来凯医药宣布任命Jeff Porter为公司科学顾问委员会主席。作为前诺华高级副总裁、诺华生物医学研究中心化学生物学和新治疗领域全球负责人,Jeff Porter拥有超过25年的全球新药研发领导和战略经验。
传奇生物任命方国伟为高级副总裁
1日,传奇生物在美国新泽西州萨默塞特正式宣布,任命方国伟博士为公司高级副总裁,研究与早期开发全球负责人。加入传奇之前,方国伟博士担任Zymeworks公司研发高级副总裁,负责新型技术平台开发及多功能生物制剂和抗体药物偶联物组合的开发。
 :收到双价人乳头瘤病毒疫苗(毕赤酵母)药品注册证书
:收到双价人乳头瘤病毒疫苗(毕赤酵母)药品注册证书
28日,沃森生物公告,公司子公司泽润生物泽润生物收到双价人乳头瘤病毒疫苗(毕赤酵母)药品注册证书。
赛诺菲酶替代疗法Xenpozyme在日本获批
今日,赛诺菲宣布,日本厚生劳动省已经批准该公司的创新酶替代疗法Xenpozyme(olipudase alfa)上市,用于治疗酸性鞘磷脂酶缺乏症(acid sphingomyelinase deficiency,ASMD)成人和儿科患者的非中枢神经系统症状。这是一种罕见的潜在致命遗传病。新闻稿指出,Xenpozyme是首个获批治疗ASMD的疗法。
:FDA将推迟F-627上市申请批复
31日,亿帆医药发布关于控股子公司在研产品F-627项目的进展公告。公告显示,亿帆医药控股子公司EviveBiotechLtd.在研产品艾贝格司亭α注射液(以下简称“F-627”)用于预防及治疗肿瘤患者在化疗过程中引起的嗜中性粒细胞减少症于2022年3月31日(美国时间2022年3月30日)收到美国FDA的邮件通知,因旅行限制,FDA将推迟F-627上市申请批复,直到现场检查完成。
治疗乳腺癌 第一三共ADC药物拟纳入突破性治疗品种
1日,CDE官网最新显示,第一三共ADC药物Trastuzumab deruxtecan(T-DXd)拟纳入突破性治疗品种,用于治疗既往接受过一种或一种以上抗HER2药物治疗的不可切除或转移性HER2阳性乳腺癌成人患者。
默沙东儿科肺炎疫苗PDUFA日期遭美国FDA推迟
日前,美国FDA宣布将延长默沙东Vaxneuvance补充生物制剂许可申请的处方药用户费用法案日期,预计将于今年7月1日做出最终决定。据悉,Vaxneuvance是一种婴儿和儿童预防性使用的15价肺炎球菌结合疫苗。
复宏汉霖首个创新型单抗H药汉斯状?获批上市
3月25日,上海—复宏汉霖宣布,旗下首款自主研发的创新生物药PD-1抑制剂H药——汉斯状?(通用名:斯鲁利单抗注射液)正式获得国家药品监督管理局(NMPA)批准,用于经既往标准治疗失败的、不可切除或转移性微卫星高度不稳定(MSI-H)的成人晚期实体瘤适应症,为患者提供治疗新选择,也为国内肿瘤精准免疫治疗赋能添势,助力推进中国生物医药行业高质量发展。
 单抗/双抗
单抗/双抗
礼来IL-13抗体3期临床结果积极
日前,礼来宣布,其在研IL-13抑制剂lebrikizumab作为单药疗法,在治疗中重度特应性皮炎患者的关键性3期临床试验中获得积极结果。在接受治疗16周之后,超过50%的患者疾病严重程度至少降低75%(EASI-75)。而且,lebrikizumab同时为瘙痒和其它重要患者报告结果带来具有临床意义的改善。
诺华2款1类生物新药在华获批临床
29日,CDE官网公示,诺华两款1类生物新药获得临床试验默示许可,分别为靶向TIM-3受体的单抗MBG453和抗TGF-β单抗NIS793,它们针对的适应症均为较低危骨髓增生异常综合征。
靶向B7H4和4-1BB!和铂医药递交新型双抗临床申请
28日,中国国家药监局药品审评中心(CDE)官网公示,和铂医药递交了HBM7008新药临床试验申请,并获得受理。公开资料显示,HBM7008是和铂医药开发的一款靶向B7H4和4-1BB的双特异性抗体,于一个月前在澳大利亚获批临床,并进入1期临床试验阶段。
康诺亚IL-4Rα单抗II期临床成功
30日,康诺亚宣布,其1类新药CM310针对慢性鼻窦炎伴鼻息肉II期临床研究达到全部疗效终点,并获得积极结果。CM310是由康诺亚自主研发的一款以人IL-4受体α亚基(IL-4Rα)为靶点的创新型人源化单克隆抗体,可选择性地与IL-4Rα相结合,阻断IL-4Rα与IL-4以及IL-13的结合从而抑制其生物学活性,从而阻断诱导慢性鼻窦炎伴鼻息肉等过敏反应的信号传导途径。
靶向Claudin18.2 信达生物双特异性抗体疗法步入临床
29日,信达生物制药集团宣布其自主研发的重组靶向紧密蛋白连接蛋白18.2(Claudin18.2,CLDN18.2)和分化抗原簇3(CD3)的双特异性抗体(研发代号:IBI389)在治疗晚期恶性肿瘤的I期临床试验中完成首例患者给药。
嘉和生物EGFR/c-Met/c-Met三特异性抗体申报临床
29日,CDE官网显示,嘉和生物EGFR/c-Met/c-Met三特异性抗体在国内的临床试验申请获国家药监局受理。GB263T是全球首个EGFR/c-Met/c-Met三特异性抗体,针对EGFR和两个不同c-Met表位。且拥有两个Fab结合EGFR,Fc片段发生了突变,增强了Fc功能。
控股孙公司BC008抗体注射液获批临床
4月1日,桂林三金发布公告称,其控股孙公司宝船生物获得了国家药监局核准签发的BC008抗体注射液的临床试验批准通知书,将开展用于CLDN18.2阳性晚期实体瘤治疗的临床试验。
先进疗法
治疗慢性乙肝 腾盛博药公布RNAi疗法2期临床最新结果
31日,腾盛博药在2022年亚太肝脏研究学会第31届会议(APASL)上,公布了其临床阶段小干扰核糖核酸(siRNA)BRII-835(VIR-2218)在中国慢性乙型肝炎病毒感染患者中进行的一项2期随机、双盲、安慰剂对照试验的最新数据。数据显示,在接受两次BRII-835(VIR-2218)给药后,中国慢性HBV感染患者的HBV表面抗原(HBsAg)水平呈剂量依赖性降低,并且在HBeAg阴性和HBeAg阳性患者中HBsAg水平降低程度相近。
子公司HRX0701片获得药物临床试验批准通知书
1日,恒瑞医药发布公告称,其子公司山东盛迪医药收到国家药监局核准签发关于HRX0701片的《药物临床试验批准通知书》,同意批准HRX0701片(Ⅰ)(50/850mg规格)、HRX0701片(Ⅱ)(50/1000mg规格)进行人体生物等效性试验和食物影响研究。
渤健/Ionis终止BIIB078一期临床试验
28日,渤健和合作伙伴Ionis Pharmaceuticals发布了BIIB078临床一期试验的一线结果。BIIB078是一种用于治疗C9orf72相关的ALS的在研反义寡核苷酸药物。一线结果显示,该药物并没有显示出临床益处,渤健和Ionis因此决定终止其临床试验。
二线治疗淋巴瘤 Yescarta获FDA批准新适应症
近日,美国FDA宣布,批准吉利德科学旗下Kite Pharma开发的CD19靶向CAR-T疗法Yescarta(axicabtagene ciloleucel)扩展适用范围,用于二线治疗大B细胞淋巴瘤(LBCL)成人患者。他们在接受一线化学免疫治疗后产生耐药性,或在接受一线疗法12个月内出现复发。这一疗法不适用于治疗原发中枢神经系统淋巴瘤患者。
重症肌无力皮下注射疗法达到3期临床终点
近日,argenx公司宣布,efgartigimod皮下注射制剂在一项3期临床试验中获得积极数据。试验达到了其主要终点,即治疗29天时,全身型重症肌无力患者的免疫球蛋白G水平较基线降低,与该药获批静脉输注制剂Vyvgart(efgartigimod alfa-fcab)相比达到非劣效性标准。
礼来公布Retevmo治疗非小细胞肺癌I/II期试验最新数据
1日,礼来在欧洲肺癌大会上公布了 Retevmo(selpercatinib 40mg和80mg胶囊)的I/II期LIBRETTO-001试验最新数据,该试验针对非小细胞肺癌RET基因融合阳性患者。试验结果显示,247例经治患者中,确认的ORR为61.1% ,中位PFS为24.9个月,中位DoR为28.6个月。69例初治患者中,确认的ORR为84.1%,中位PFS为22个月,DoR为 20.2个月。26例存在基线脑转移的患者经过Retevmo治疗后,CNS-ORR为84.6%,中位PFS为19.4个月,其中22例患者确认为完全缓解或部分缓解。
 京东健康2021年亏损10.7亿元 同比减少93.8%
京东健康2021年亏损10.7亿元 同比减少93.8%
28日,京东健康发布2021年财报。2021年收入306.8亿元,同比增58.3%;年度亏损10.7亿元,亏损额同比减少93.8%;非国际财务报告准则盈利14.02亿元,同比增91.5%。
一季度净利预计同比增长585%-692%
28日,奥泰生物公告,预计2022年第一季度实现净利润10.3亿元-11.9亿元,同比增加585.40%至691.87%,新冠检测业务订单继续保持稳定增长。
2021年收入14.24亿元 维迪西妥单抗8400万元
29日,荣昌生物公布2021年财报,公司全年收入14.24亿元,净利润2.76亿元,研发投入7.11亿元。值得注意的是,3月31日,荣昌生物将在科创板二度IPO上市,募集资金约26亿元。
天境生物2021年营收8800万元
3月29日,天境生物发布2021年财报。财报显示,2021年公司营收为8800万元;亏损额为23.315亿元,账上现金及现金等价物约为43亿元。研发费用为12.130亿元,上年同期9.847亿元。截至2021年12月31日,天境生物拥有现金、现金等价物和短期投资43亿元。
2021年净利润3.52亿元 同比增长53.1%
28日,昊海生科公布2021年年度报告,公司实现营业收入17.67亿元,同比增长32.61%;归母净利润3.52亿元,同比增长53.1%;基本每股收益2元。公司拟向全体股东每10股派发现金红利7元(含税)。营收增长主要是随着国内新冠肺炎疫情得到有效控制,新冠疫情对本集团经营活动的影响逐渐减弱,本集团各产品线收入均实现大幅增长所致。
2022年Q1净利润同比预增51.97%-63.66%
28日,特宝生物公告,预计2022年第一季度实现归母净利润为5200万元到5600万元,同比增加51.97%到63.66%。报告期内公司积极开拓市场,派格宾等主营业务产品的销售收入持续上升,净利润实现稳步增长。
 熙源安健完成亿元级天使轮融资
熙源安健完成亿元级天使轮融资
28日,疼痛治疗领域创新药物研发新锐公司熙源安健医药(上海)有限公司宣布已完成亿元级天使轮融资。本轮融资由启明创投和博远资本共同领投,健壹资本跟投,所募资金将用于疼痛治疗研发管线的推进、创新技术产品的合作开发和并购引进等。
凝生物完成近亿元Pre-A轮融资
4月1日,科凝生物制药(深圳)有限公司宣布完成近亿元Pre-A轮融资。此轮融资由龙磐投资领投,凯泰资本及老股东清科创投跟投。此轮融资将用于支持科凝在眼科、骨科等现有创新管线的临床前开发,并以技术平台为基础,加速建构后续研发管线。
 “RNA诊断第一股”科创板上市 开盘破发
“RNA诊断第一股”科创板上市 开盘破发
30日,“RNA诊断第一股”仁度生物在上海证券交易所科创板上市,发行价格为72.65元/股,开盘破发,跌6.4%,报68元。当日收盘报64.76元/股,跌10.86%。
联影医疗拟科创板上市 拟募集124.8亿元
2日,国产医学影像设备巨头上海联影医疗科技股份有限公司计划在上交所科创板上市,拟募集资金124.8亿元。联影医疗本次IPO实行超额配售权机制,最多发行不超过1.15亿股,募资金额不低于124.8亿元。其发行前总股本为7.24亿股,若以发行不超1亿股粗略计算,该公司估值有望达到千亿元之上。
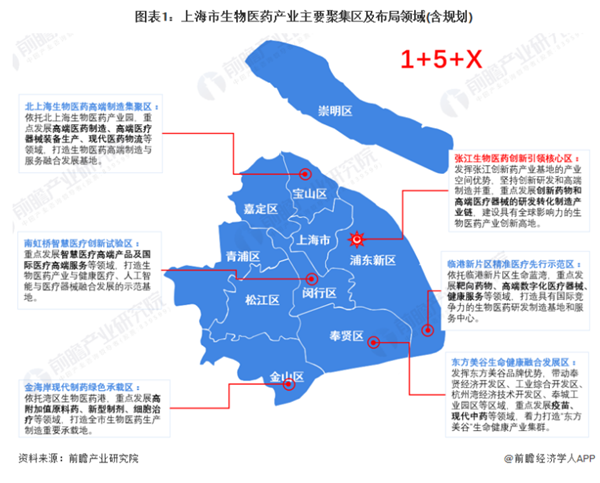
 上海市生物医药产业空间布局
上海市生物医药产业空间布局
生物医药产业是上海市九大战略性新兴产业之一,也是上海市三大重点产业之一,近年来,上海市在一应政策的指导下加快了生物医药产业布局,已逐渐形成了以张江生物医药创新引领核心区为轴心,以临港新片区精准医疗先行示范区、东方美谷生命健康融合发展区、金海岸现代制药绿色承载区、北上海生物医药高端制造集聚区和南虹桥智慧医疗创新试验区为依托的“1+5+x”生物医药产业空间布局。
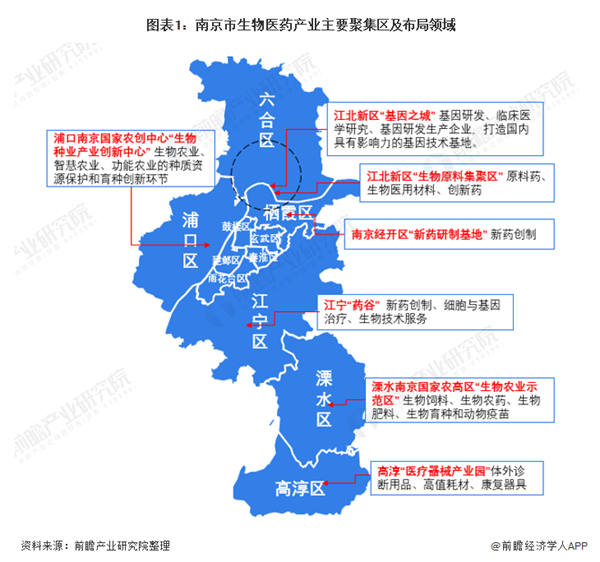
 南京市生物医药产业空间布局
南京市生物医药产业空间布局
近年来,南京依托生物经济优势,大力推动主导产业发展,形成了江北新区“基因之城”、江北新区“生物原料集聚区”、江宁“药谷”、南京经开区“新药研制基地”等多生物医药产业聚集区:
 从学术到产业,更多定制化产业周刊(全球产业舆情监测、前沿技术情报追踪、产融政策权威解读、产业招商精准线索),敬请拨打400-068-7188。同时前瞻产业研究院还提供产业大数据、产业研究、产业链咨询、产业图谱、产业规划、园区规划、产业招商引资、IPO募投可研、IPO业务与技术撰写、IPO工作底稿咨询等解决方案。
从学术到产业,更多定制化产业周刊(全球产业舆情监测、前沿技术情报追踪、产融政策权威解读、产业招商精准线索),敬请拨打400-068-7188。同时前瞻产业研究院还提供产业大数据、产业研究、产业链咨询、产业图谱、产业规划、园区规划、产业招商引资、IPO募投可研、IPO业务与技术撰写、IPO工作底稿咨询等解决方案。