干货!传奇生物公布实体瘤、同种异体CAR-T疗法最新进展(附PPT)
▎药明康德内容团队编辑
今日,传奇生物在研发日(R&D Day)活动上,介绍了该公司细胞疗法开发的最新布局和动态。传奇生物与杨森(Janssen)合作开发的靶向B细胞成熟抗原(BCMA)的CAR-T疗法cilta-cel,已经在治疗多发性骨髓瘤的临床试验中表现出卓越的抗癌活性。它已经获得美国FDA授予的优先审评资格,有望在11月底获得批准上市。
在今天的研发日活动上,传奇生物的高管不但介绍了cilta-cel的最新研发布局,而且详述了该公司在治疗实体瘤方面的重点研发项目,以及在构建创新同种异体CAR-T疗法技术平台方面的突破。
 克服CAR-T疗法治疗实体瘤的障碍
克服CAR-T疗法治疗实体瘤的障碍
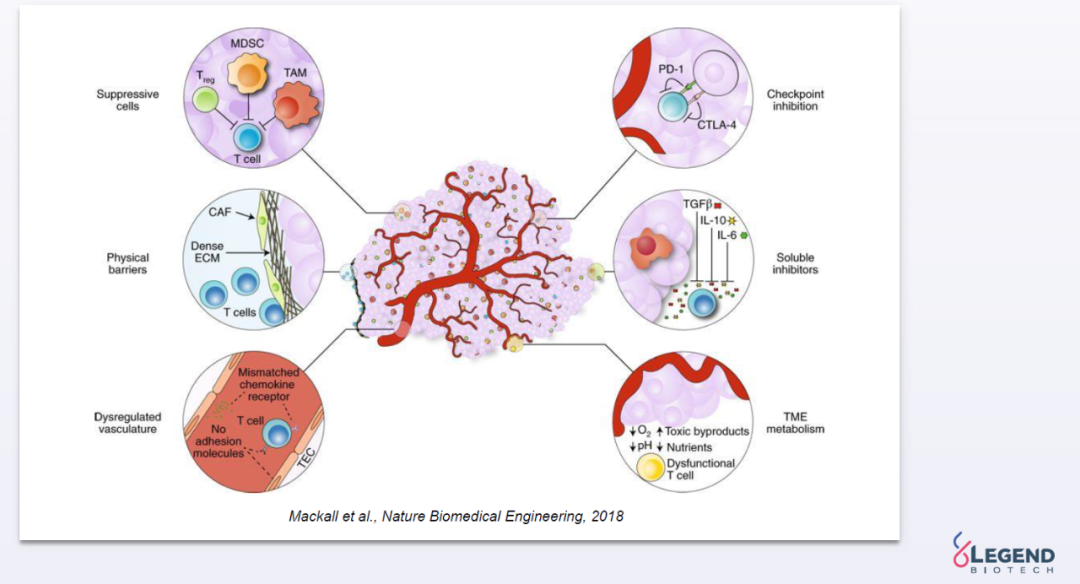
CAR-T疗法虽然在治疗血液恶性肿瘤方面获得显著进展,但是在治疗实体瘤方面还未获得同样的疗效。这是因为实体瘤的肿瘤微环境中存在多种抑制T细胞活性的免疫抑制细胞和细胞因子,而且找到在实体瘤中特异性表达,而在健康组织中不表达的抗原并不容易。因此,开发靶向实体瘤的CAR-T疗法需要在疗法设计上做出多种优化。
 治疗胃癌和胰腺癌的CAR-T疗法
治疗胃癌和胰腺癌的CAR-T疗法
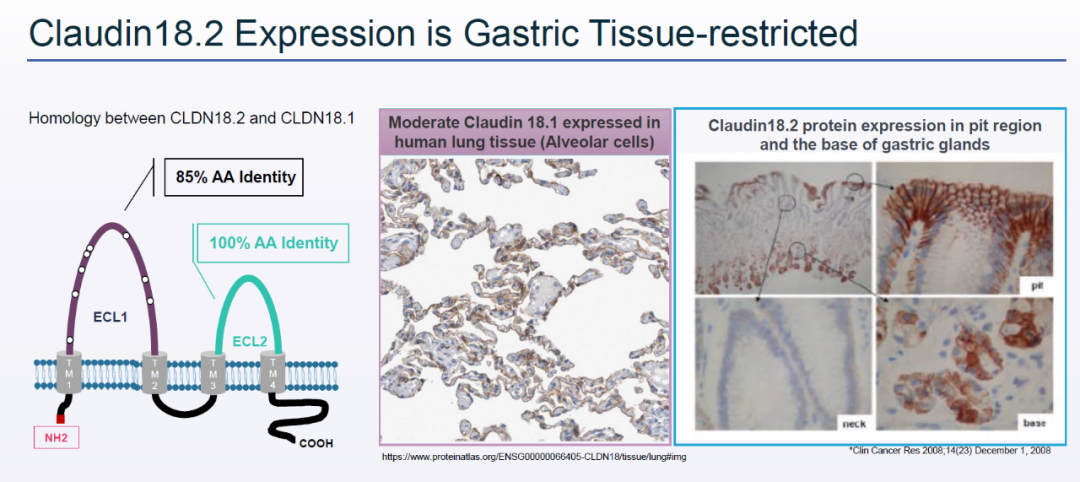
传奇生物的LB1908是一款靶向Claudin18.2(CLDN18.2)的CAR-T疗法。CLDN18.2在胃癌、胰腺癌等癌症类型中表达,是目前抗癌药物开发的热门靶点。然而与它同源性很高的CLDN18.1在人体的肺组织中表达。这意味着,CAR-T疗法需要对CLDN18.2具有高度特异性,否则有可能攻击健康肺组织,导致严重毒副作用。
 传奇生物开发的VHH抗体平台利用了羊驼类动物体内产生的只包含重链的纳米抗体。这种抗体因为没有传统的轻链,比人体产生的抗体更为小巧,但是可以和传统抗体一样与抗原紧密结合。VHH抗体只包含了纳米抗体的可变区片段,它不但可以特异性结合传统抗体无法结合的创新表位,而且多个不同的VHH连接在一起还可以同时靶向多个不同抗原。
传奇生物开发的VHH抗体平台利用了羊驼类动物体内产生的只包含重链的纳米抗体。这种抗体因为没有传统的轻链,比人体产生的抗体更为小巧,但是可以和传统抗体一样与抗原紧密结合。VHH抗体只包含了纳米抗体的可变区片段,它不但可以特异性结合传统抗体无法结合的创新表位,而且多个不同的VHH连接在一起还可以同时靶向多个不同抗原。
 LB1908利用了VHH抗体设计确保了它对CLDN18.2具有高度的特异性。在临床前胃癌和胰腺癌的动物模型中,它都表现出强力的抗癌活性。
LB1908利用了VHH抗体设计确保了它对CLDN18.2具有高度的特异性。在临床前胃癌和胰腺癌的动物模型中,它都表现出强力的抗癌活性。
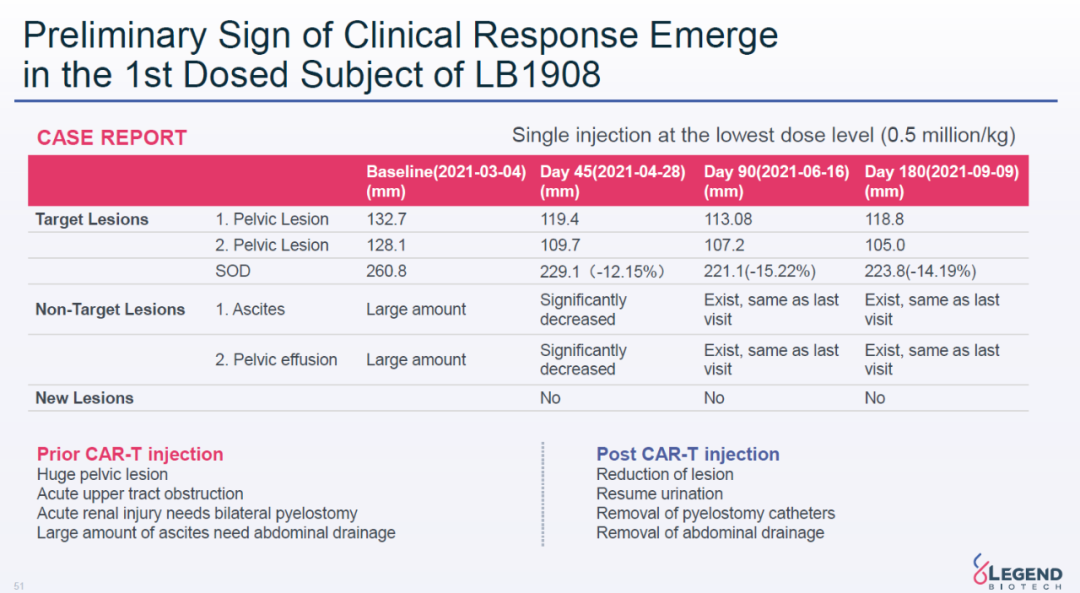
 目前,这款在研CAR-T疗法已经进入剂量递增1期临床试验。在首例接受最低剂量LB1908治疗的患者中,它表现出良好的安全性和初步抗癌活性。在接受治疗180天后,患者疾病稳定,而且在骨盆的肿瘤缩小15%,位于身体其它部位的病灶显著缩小,患者的生活质量也获得显著提高。
目前,这款在研CAR-T疗法已经进入剂量递增1期临床试验。在首例接受最低剂量LB1908治疗的患者中,它表现出良好的安全性和初步抗癌活性。在接受治疗180天后,患者疾病稳定,而且在骨盆的肿瘤缩小15%,位于身体其它部位的病灶显著缩小,患者的生活质量也获得显著提高。
 传奇生物计划进一步扩展在中国的临床试验,并且正在准备向美国FDA递交这一疗法的IND申请。
传奇生物计划进一步扩展在中国的临床试验,并且正在准备向美国FDA递交这一疗法的IND申请。
克服肿瘤微环境阻碍的“武装”CAR-T疗法
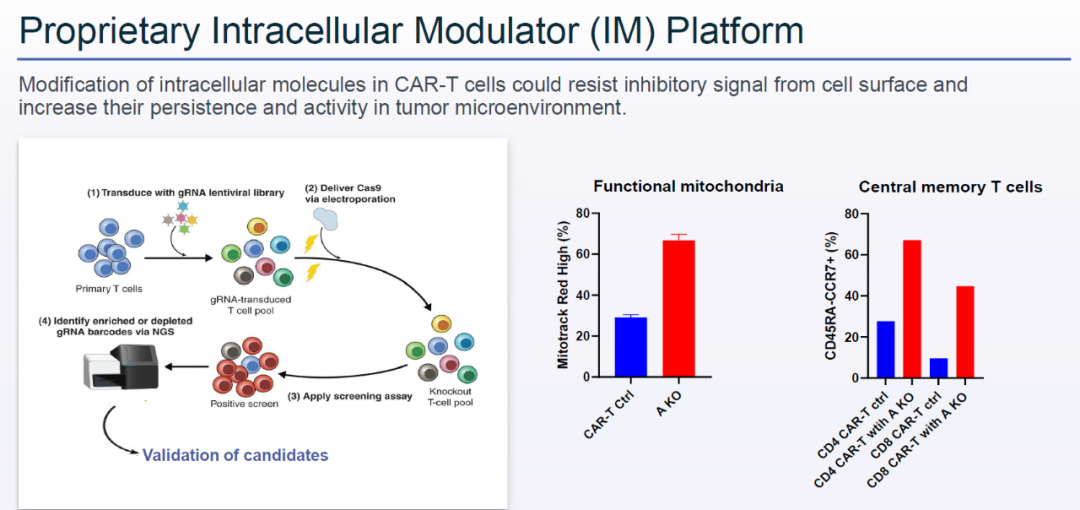
为了克服肿瘤微环境中免疫抑制因素对CAR-T活性的影响,传奇生物独有的技术平台大规模筛选让CAR-T细胞抵抗免疫抑制信号的细胞内靶点,利用它们提高疗法在肿瘤微环境中的持久性和活性。
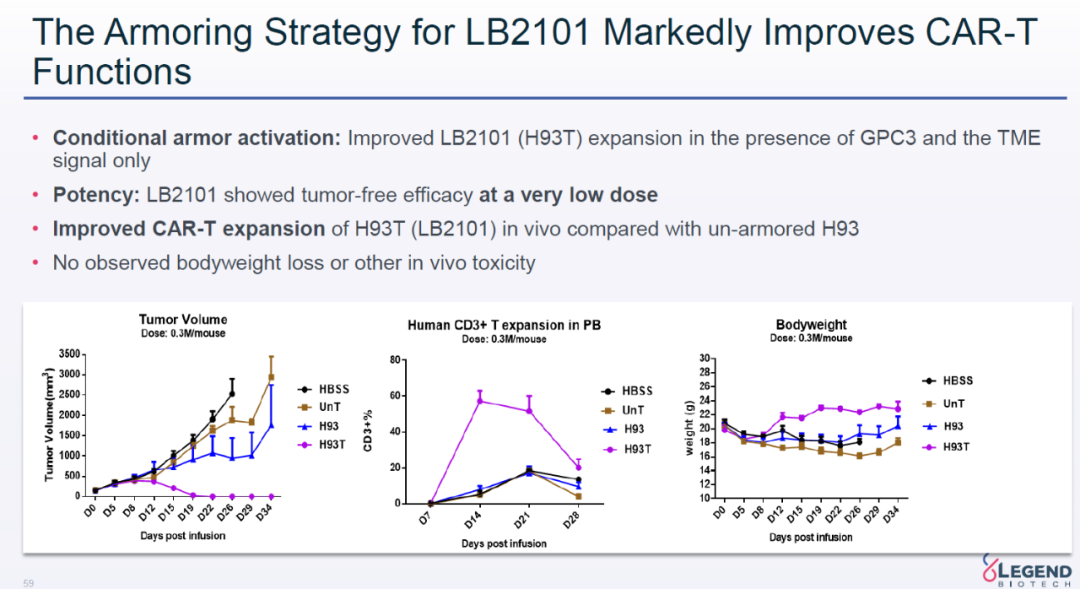
 该公司开发的LB2101是一款靶向GPC-3的“武装”(armored)CAR-T疗法。它在表达靶向GPC-3的嵌合抗原受体(CAR)以外,还同时表达着一个被肿瘤微环境中的信号激活的跨膜蛋白。它只有在CAR信号通路被激活的同时才能被肿瘤微环境中的信号激活,因此不会影响CAR-T细胞的特异性。它可以改善CAR-T细胞的浸润、增殖和持久性。
该公司开发的LB2101是一款靶向GPC-3的“武装”(armored)CAR-T疗法。它在表达靶向GPC-3的嵌合抗原受体(CAR)以外,还同时表达着一个被肿瘤微环境中的信号激活的跨膜蛋白。它只有在CAR信号通路被激活的同时才能被肿瘤微环境中的信号激活,因此不会影响CAR-T细胞的特异性。它可以改善CAR-T细胞的浸润、增殖和持久性。
 ▲LB2101简介(图片来源:传奇生物官网)
▲LB2101简介(图片来源:传奇生物官网)
在动物实验中,这款疗法与没有“武装”起来的CAR-T疗法相比,显示出更高的抗癌活性,而且在动物体内的细胞扩增幅度更大。
 治疗小细胞肺癌的CAR-T疗法
治疗小细胞肺癌的CAR-T疗法
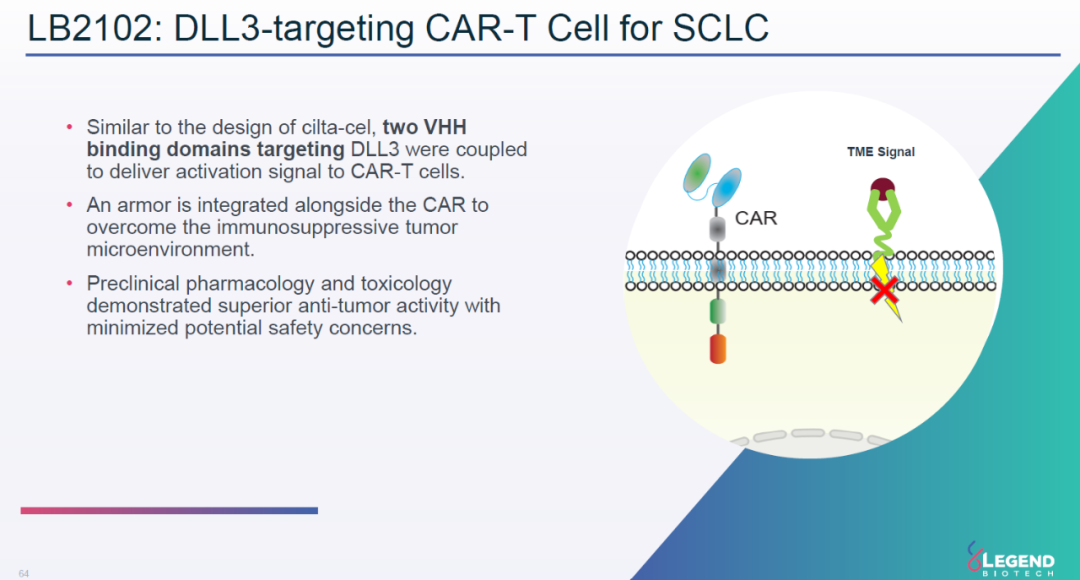
LB2102是一款靶向DLL3的CAR-T疗法。DLL3是一种在小细胞肺癌(SCLC)和某些神经内分泌肿瘤中广泛表达的潜在靶点。LB2102使用了VHH抗体技术和克服肿瘤微环境抑制因素的“武装”CAR-T技术。它携带着两个识别DLL3的VHH抗体片段,和一个能被肿瘤微环境中信号激活的跨膜蛋白。
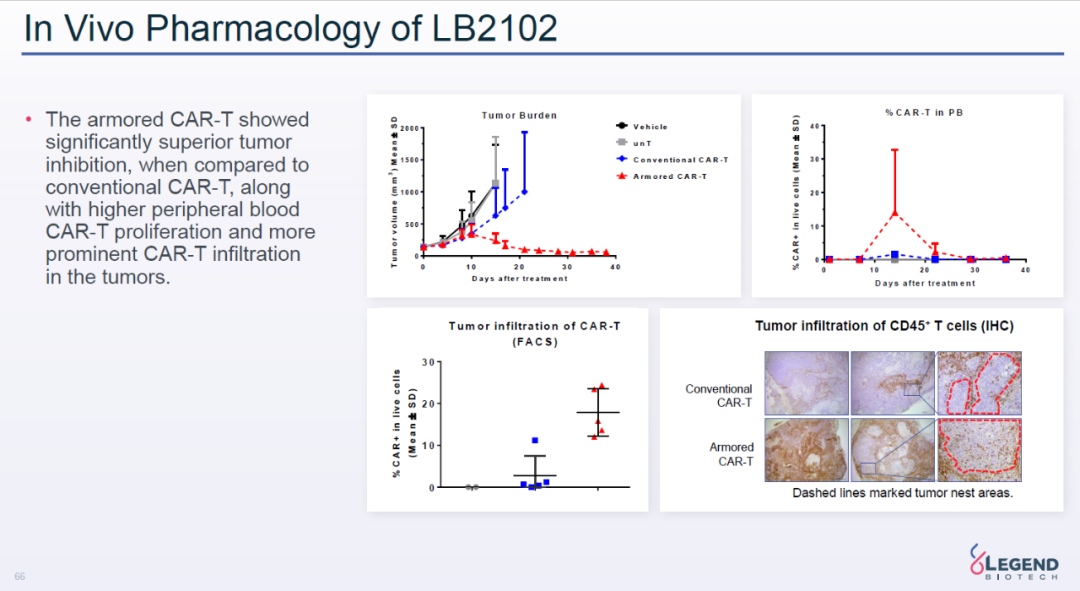
 临床前体内研究显示,这一疗法与传统CAR-T疗法相比,更有效地缩小肿瘤,而且外周血中的CAR-T细胞和浸润肿瘤的CAR-T细胞数目都显著提升。
临床前体内研究显示,这一疗法与传统CAR-T疗法相比,更有效地缩小肿瘤,而且外周血中的CAR-T细胞和浸润肿瘤的CAR-T细胞数目都显著提升。
 不使用基因编辑的同种异体CAR-T技术平台
不使用基因编辑的同种异体CAR-T技术平台
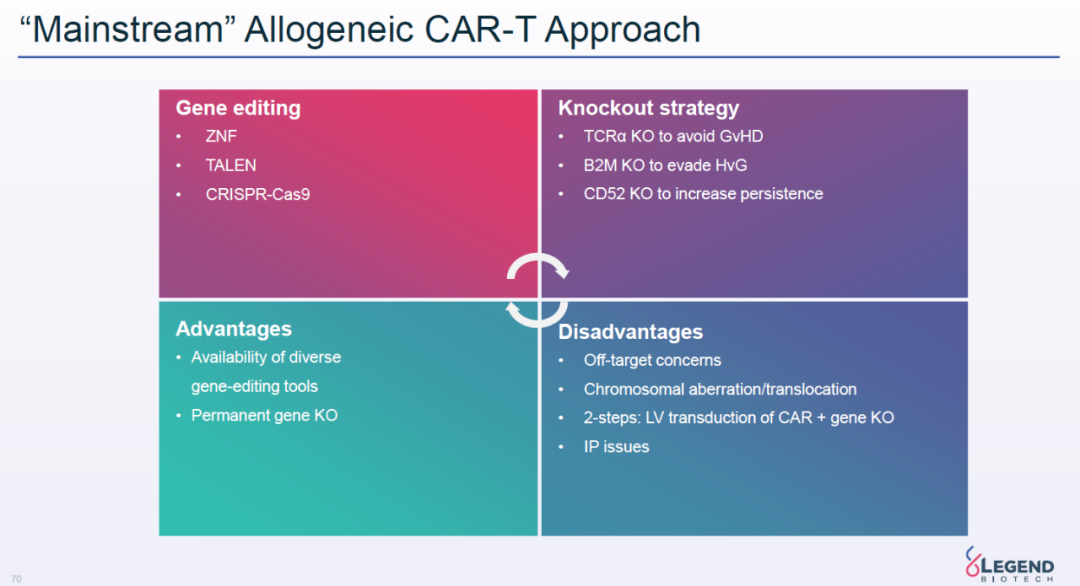
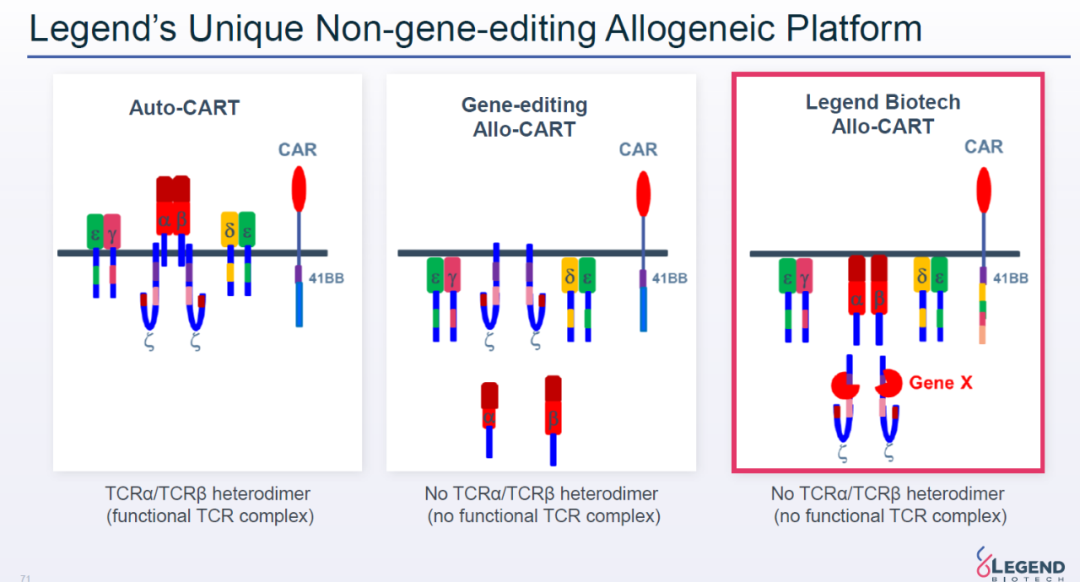
同种异体CAR-T细胞疗法需要克服的一个重要障碍是移植到患者体内的T细胞攻击宿主的组织,以及宿主对外来细胞的免疫排斥。目前,大多数同种异体CAR-T疗法利用基因编辑来敲除T细胞中的内源性T细胞受体(TCR)以及其它可能引发宿主免疫排斥的蛋白。这一疗法虽然可以使用多种基因编辑工具,永久性敲除引发免疫排斥反应的蛋白,但是它也有一些潜在隐患,包括基因编辑工具的脱靶效应,以及潜在染色体异常风险。染色体异常风险也导致近日的一项同种异体CAR-T疗法临床试验被FDA叫停。
 传奇生物的开发策略是开发在细胞内与TCR亚基结合的蛋白,它们与TCR的α和β亚基结合之后,阻碍正常TCR复合体的形成,从而阻断内源性TCR信号的传播。这种策略不需要对细胞进行基因编辑,而且阻断内源性TCR信号的蛋白可以由携带CAR转基因的病毒载体同步表达,减少了CAR-T疗法的生产步骤。
传奇生物的开发策略是开发在细胞内与TCR亚基结合的蛋白,它们与TCR的α和β亚基结合之后,阻碍正常TCR复合体的形成,从而阻断内源性TCR信号的传播。这种策略不需要对细胞进行基因编辑,而且阻断内源性TCR信号的蛋白可以由携带CAR转基因的病毒载体同步表达,减少了CAR-T疗法的生产步骤。
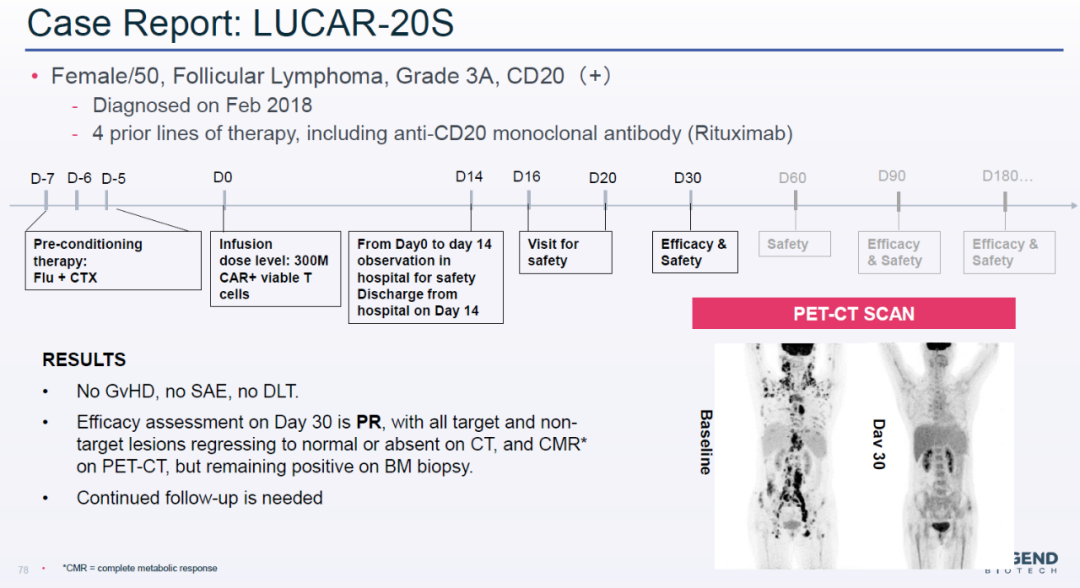
 利用这一平台开发的CAR-T疗法LUCAR-20S已经进入1期临床试验。目前已经有5名复发/难治性非霍奇金淋巴瘤患者接受给药。其中3名患者(60%)获得部分缓解,尚未发现剂量限制毒性。其中一名患者在接受治疗30天后,放射性成像检测显示所有病灶几乎完全消失,骨髓活检仍为阳性,因此被判定为部分缓解。
利用这一平台开发的CAR-T疗法LUCAR-20S已经进入1期临床试验。目前已经有5名复发/难治性非霍奇金淋巴瘤患者接受给药。其中3名患者(60%)获得部分缓解,尚未发现剂量限制毒性。其中一名患者在接受治疗30天后,放射性成像检测显示所有病灶几乎完全消失,骨髓活检仍为阳性,因此被判定为部分缓解。
 Cilta-cel的未来研发计划
Cilta-cel的未来研发计划
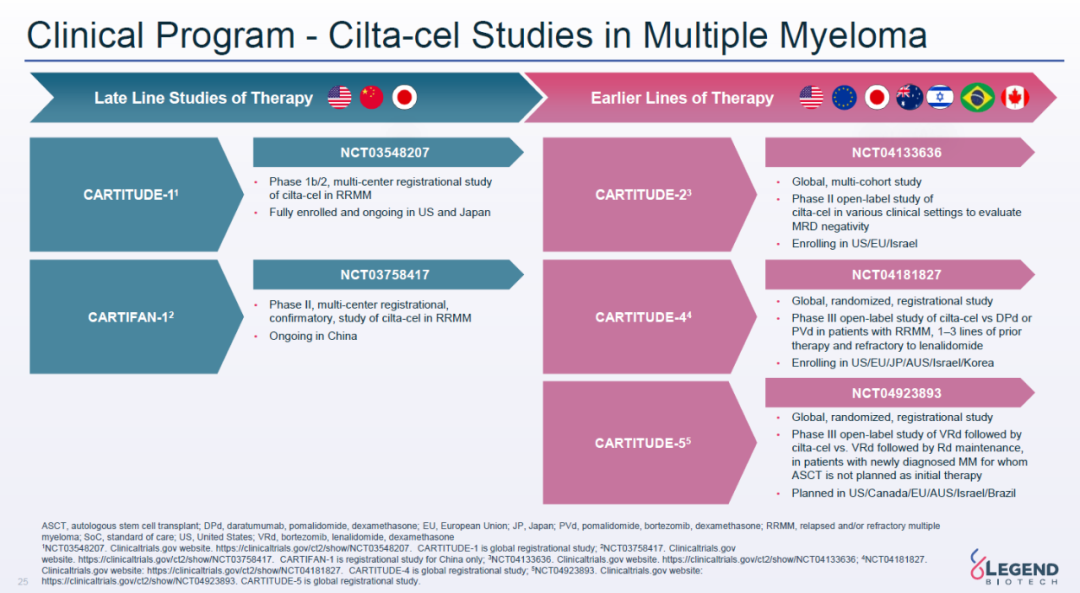
靶向BCMA的cilta-cel已经在接受过多种前期疗法的多发性骨髓瘤患者表现出卓越的疗效。在研发日上,传奇生物介绍了cilta-cel的进一步临床开发计划。该公司与杨森合作,已经启动2期临床试验,在接受过1-3种前期疗法治疗的多发性骨髓瘤患者中评估cilta-cel的效力。同时,两项关键性3期临床试验已经启动,旨在评估cilta-cel作为一线疗法和二线疗法治疗多发性骨髓瘤患者的潜力。
 在研发日上,传奇生物还介绍了该公司在开发CAR自然杀伤细胞(CAR-NK)方面的布局。限于篇幅,本文不做详细介绍。向药明康德微信号回复“传奇生物”(如下图)即可获得链接信息,浏览研发日PPT报告。
在研发日上,传奇生物还介绍了该公司在开发CAR自然杀伤细胞(CAR-NK)方面的布局。限于篇幅,本文不做详细介绍。向药明康德微信号回复“传奇生物”(如下图)即可获得链接信息,浏览研发日PPT报告。
参考资料:
[1] Legend Biotech R&D Day. Retrieved October 18, 2021, from https://investors.legendbiotech.com/static-files/3cb06824-4ee5-4610-951c-8a3bd8e9ec3b
[2] U.S. Food and Drug Administration Grants BCMA CAR-T Cilta-cel Priority Review for the Treatment for Relapsed/Refractory Multiple Myeloma. Retrieved October 18, 2021, from https://investors.legendbiotech.com/news-releases/news-release-details/us-food-and-drug-administration-grants-bcma-car-t-cilta-cel
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。